SRRF-Stream ( Andor )
SRRF Stream+ Super-Resolution Microscopy Software
'SRRF-Stream+'는 표준 현미경의 이미징 성능을 대폭 강화하는 실시간 초고해상도 현미경 기능입니다. 이전에는 전용 하이엔드 초고해상도 현미경으로만 가능했던 수준의 해상도를 달성할 수 있습니다. 'SRRF' 기술(초해상도 방사형 변동)을 기반으로 하는 SRRF-Stream+는 초해상도에 대한 쉽고 유연한 소프트웨어 접근 방식을 제공합니다.
NEW – 이제 ZL41 Cell, Sona 및 일부 Zyla 4.2 PLUS 카메라에 사용할 수 있어 이 놀라운 기술을 더욱 저렴한 가격대로 더 많은 애플리케이션에 사용할 수 있습니다!
- 향상된 해상도 - 회절의 장벽 너머를 확인하세요! 최대 100nm 해상도(2~6배 개선)로 인사이트가 향상됩니다.
- 실시간 - 향상된 워크플로로 후처리가 필요 없습니다. '라이브 모드'에서 보기.
- 세포 친화적 - 낮은 여기 강도(mW-W/cm2)로 살아있는 세포 관찰을 연장하고 정확한 생리학을 유지합니다.
- 기존 형광 표지자와 함께 사용하기 쉬움 - 일반적인 라벨링 프로토콜과 GFP와 같은 라벨을 사용합니다.
- 라이브 세포 역학 - iXon EMCCD로 1~2초마다 전체 FOV 초고해상도 이미지를 제공합니다. > ROI를 사용하여 10fps 이상.
- 비용 효율적 - 기존 형광 현미경을 초고해상도 현미경으로 전환합니다.
과학에는 발견과 지식의 발전을 제약하는 물리 법칙에 따른 한계가 있습니다. 21세기 초까지만 해도 현미경 관찰에서 빛의 회절 한계는 넘을 수 없는 장벽이었습니다. 이 물리학 법칙에 따르면 두 점이 보는 데 사용되는 빛의 파장의 절반보다 더 가까우면 두 점을 해상도(명확하게 분리)로 확인할 수 없었습니다. 실제로 이것은 광학 현미경이 200nm 이상 떨어져 있는 물체/구조물만 분해할 수 있다는 것을 의미합니다. 따라서 많은 아세포 구조와 세포 소기관이 200nm보다 작기 때문에 200nm의 장벽은 밝혀지지 않은 상당한 지식의 공백을 남깁니다.
21세기의 첫 10년 동안 여러 가지 독창적인 현미경 기술을 통해 빛의 회절 한계가 극복되었습니다. 새로운 발견의 영역이 열릴 준비가 된 것이죠. 초고해상도를 위한 여러 가지 방법이 발전하여 빛의 회절 한계를 뛰어넘는 이미지가 가능해졌습니다. STED(자극 방출 고갈 현미경), STORM/PALM(확률적 광학 재구성 현미경)/(형광 광 활성화 국소화 현미경), SIM(구조 조명 현미경)과 같은 초고해상도 현미경 방법이 연구자들에게 제공되었습니다.
초고해상도 방법은 새로운 발견의 장을 열었지만, 이러한 방법에는 몇 가지 한계가 존재했습니다. 복잡한 샘플 준비, 긴 수집 시간, 수집에 필요한 높은 에너지 요구 사항으로 인해 이러한 기술은 라이브 세포 이미징에 사용하기에 부적절합니다(호환되지 않는 것은 아니지만). 또한 광학 요구 사항과 컴퓨터 성능이 필요하기 때문에 이러한 SR 방법은 매우 비싸고 많은 실험실에서 접근하기 어렵습니다.
광학 오버샘플링과 컴퓨터 재할당을 결합한 스피닝 디스크 공초점 기술의 최근 발전은 회절 한계를 넘어 1.6배의 개선을 달성하고 라이브 셀 이미징에 적합하지만, 시야가 줄어들고 낮은 기본 해상도에서 시작한다는 상당한 비용이 발생한다는 단점이 있습니다. 또한 여전히 고가의 하드웨어와 불가분의 관계에 있습니다.
핀홀 크기와 맞춤형 핀홀 피치 분리의 독특한 조합을 갖춘 드래곤플라이 회전 디스크 공초점은 기본 축 및 측면 해상도가 개선되어 일상적인 이미징에 더 나은 해상도를 제공합니다. 그런 다음 획득한 이미지에서 광자 재할당(디컨볼루션)을 사용하여 잠자리의 최종 축 및 측면 해상도를 각각 240nm와 139nm로 높일 수 있습니다.
하지만 연구자에게 더 높은 해상도가 필요하다면 어떻게 해야 할까요? 또는 스피닝 디스크 공초점 현미경이 없으신가요? 빠르고 라이브 이미징과 호환되며 전체 시야각에서 초고해상도 이미지를 획득할 수 있고 필요한 경우 세포 내부 깊숙한 곳까지 관찰할 수 있는 대체 방법이 있을까요? 이 질문에 대한 답은 '예'입니다. SRRF 또는 SRRF-Stream+를 사용하면 됩니다. (Figure 1).
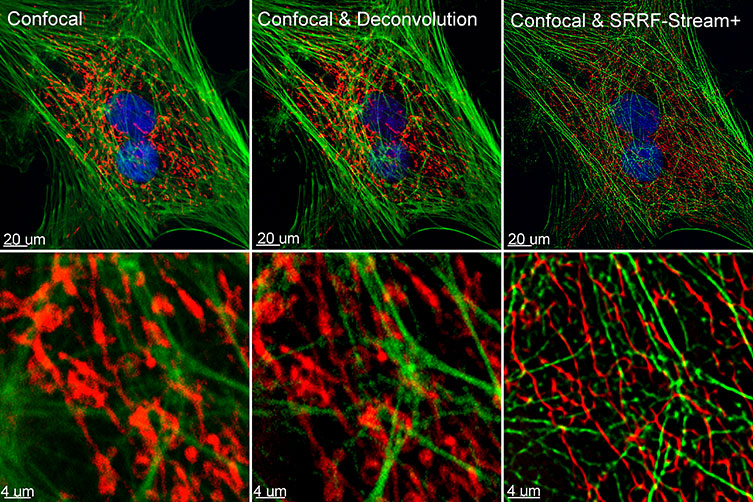
Figure 1 – Comparison between confocal imaging, confocal imaging & deconvolution and confocal imaging & SRRF-stream+. High magnification close ups are present for a better visualisation of the obtained resolution. BPA cells stained with phalloidin, mitotracker and DAP image with Ixon 888 in confocal mode (no SRRF) and confocal mode with SRRF-stream+.
2016년에 Henriques 연구실에서는 초해상도에 대한 대안적 접근 방식인 SRRF(초해상도 방사형 변동(1))를 개발했습니다. SRRF는 광시야, TIRF 또는 공초점과 결합할 수 있으며, 최종 해상도는 수집된 데이터 세트의 특성에 따라 달라집니다. 연구자들은 SRRF 알고리즘을 사용하여 최대 50nm의 XY 해상도를 달성할 수 있습니다(1). 또한 SRRF 알고리즘은 기존의 형광 물질 및 형광 단백질과 호환되기 때문에 특별한 샘플 전처리나 특별한 형광 물질이 필요하지 않으며, 수집을 위해 특별한 형광 물질이 필요하지 않습니다.
가장 중요한 것은 평균 20~100프레임(프레임이 많을수록 해상도가 향상됨)을 캡처하여 초고해상도 SRRF 이미지를 얻을 수 있으며, 이 이미징에 필요한 에너지가 cm2당 mW~W 정도이므로 SRRF가 라이브 셀 이미징과 호환된다는 점입니다. (1, 2) SRRF는 처음에 ImageJ 플러그인으로 제공되었습니다. SRRF 이미지를 얻기 위해서는 긴 획득 워크플로우가 필요했고, 획득한 데이터를 이미지J 플러그인인 NanoJ에서 획득 후 처리하여 SRRF 이미지를 얻었습니다.
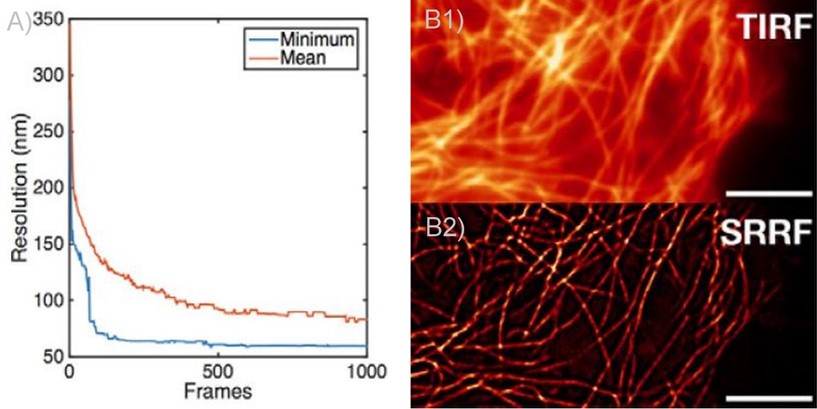 Figure 2 - SRRF and SRRF-stream resolution increase with the number of frames acquired (and processed) per time point. A) Graph presenting the resolution increase with the increasing number of acquired frames. As it can be observed there is a high increase up until 100 frames. Mean presents the average of all radial fluctuation correlation analysed (in different Regions of interest - ROI). Minimum shows the maximum resolution achieved for a given ROI. B1 and B2) Actin filaments imaged on Andor Dragonfly using TIRF (B1)) and TIRF with on the fly SRRF-stream processing (B2). It can be observed even when acquiring in TIRF modality, that SRRF-Stream provides a significant increase in resolution.
Figure 2 - SRRF and SRRF-stream resolution increase with the number of frames acquired (and processed) per time point. A) Graph presenting the resolution increase with the increasing number of acquired frames. As it can be observed there is a high increase up until 100 frames. Mean presents the average of all radial fluctuation correlation analysed (in different Regions of interest - ROI). Minimum shows the maximum resolution achieved for a given ROI. B1 and B2) Actin filaments imaged on Andor Dragonfly using TIRF (B1)) and TIRF with on the fly SRRF-stream processing (B2). It can be observed even when acquiring in TIRF modality, that SRRF-Stream provides a significant increase in resolution.
2018년 안도르와 헨리케스 교수의 협업 끝에 안도르는 SRRF-Stream을 출시했습니다. SRRF-Stream은 버튼 클릭 한 번으로 초고해상도 이미지를 즉시 전송하는 SRRF 알고리즘을 Andor가 구현한 것입니다. 원래의 SRRF 알고리즘과 마찬가지로 SRRF-Stream의 해상도는 특정 시점당 캡처되는 프레임 수에 따라 향상됩니다. 이는 100프레임까지 가장 두드러지며, 100프레임에서 500프레임까지는 보다 안정적으로 증가하고 500프레임 이후부터는 해상도가 매우 완만하게 향상됩니다(그림 2, 3). 노출 시간, 나이퀴스트 샘플링, 방사형 배율 및 링 반경 증가와 같은 다른 요소도 해상도에 영향을 미치므로 결과를 최적화하려면 이러한 요소를 테스트해야 합니다.
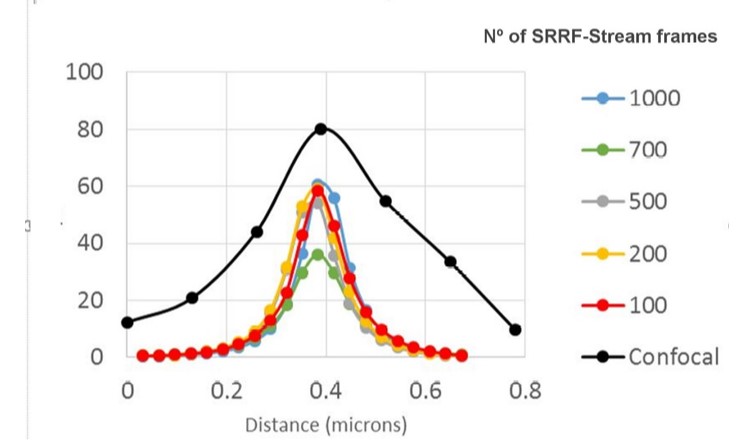
Figure 3 - SRRF-stream resolution increase with the number of frames acquired per time point. 100 nm tetraspeck beads where imaged and the FWHM was measured. We can observe that with 100 SRRF frames acquired the FMHW of the tertaspeck beads is 100 nm. The 100 nm bead can be accurately measured using the SRRF-stream algorithm and acquiring 100 frames. Images were acquired in confocal mode, and in confocal mode with different SRRF-stream acquired image images per point, respectively: 100, 200, 500, 700, 1000. Thanks to Dr Ann Wheeler, Head of the Advanced Imaging Resource at the MRC Institute of Genetics and Molecular Medicine, University of Edinburgh.
ANDOR의 SRRF-Stream은 커버 슬립 상단을 넘어 세포나 조직 내부 깊숙한 곳까지 살아있는 세포의 초고해상도, 초고해상도를 구현할 수 있도록 크게 개선되었습니다.
SRRF-Stream은 iXon Life 및 Ultra EMCCD, Sona 시리즈의 sCMOS 카메라 및 sCMOS ZL41과 함께 사용할 수 있습니다. SRRF-Stream은 Dragonfly 공초점용 제어 소프트웨어인 마이크로 매니저와 Fusion을 통해 사용할 수 있습니다. SRRF-Stream의 장점은 다음과 같습니다(3,4):
- 실시간 초고해상도 이미지로 워크플로우를 개선하고 후처리를 피할 수 있습니다.
- 사용하는 이미징 모드(예: 광시야, 공초점 또는 TIRF)와 실험 조건에 따라 최종 해상도(50-150nm)가 2~6배 증가한 초고해상도 이미지를 제공하여 빛의 회절 한계를 극복합니다.
- 이미징에 낮은 여기 전력 강도(mW ~ W/cm2)를 사용하여 세포 생리학에 미치는 영향을 최소화하면서 장시간 살아있는 세포 관찰에 대한 호환성을 높입니다.
- 기존 형광 발광체 및 형광 단백질과 호환됩니다.
- 간편한 시료 준비.
따라서 SRRF-stream은 모든 현미경을 초고해상도 현미경으로 변환할 수 있으므로 모든 현미경에 적합한 비용 효율적인 솔루션입니다. SRRF-stream은 모든 이미징 방식, 즉 와이드필드, TIRF 및 공초점 현미경과 호환됩니다. (Figure 4).
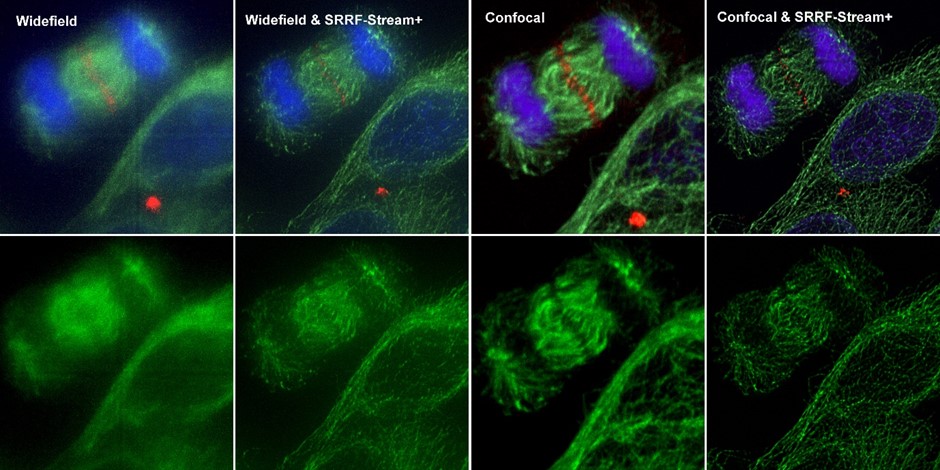
Figure 4 – Comparison between different imaging modes (widefield and Confocal) with and without SRRF-Stream+ Hela cells stained for MLKP1(red), a-tubulin(green-microtubules) a and DAPI (blue-DNA) were image in the Dragonfly with an Ixon888 camera.
2020년 7월에 SRRF-Stream 알고리즘에 대한 추가 개선 사항을 발표했습니다: SRRF-Stream+(그림 1, 4, 5, 6, 7).
SRRF-Stream+는 한 단계 더 나아가 방사형 측정값을 증가시켰습니다. 이전 버전의 SRRF에서는 반경도 측정이 6방향으로 계산되었지만 이제는 24방향으로 계산됩니다(그림 5). 이 향상된 기능으로 초고해상도 처리 데이터의 결과가 향상되며, 특히 키네토코어와 같은 원형 구조에서 간혹 보이던 별 인공물이 이제 제거됩니다. (Figure 7).
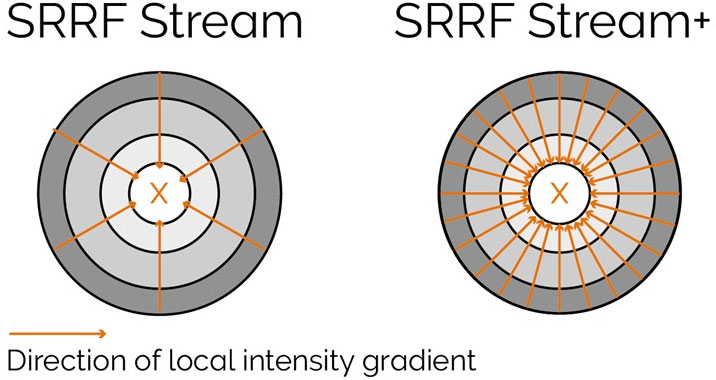
Figure 5 – Radiality computation measurements in SRRF-Stream and SRRF-Stream+ As it can be observed by the image the increased computational radiality measurements will deliver a more accurate result of the SRRF image.
SRRF-Stream+를 최대한 활용하려면 이전과 마찬가지로 사용자가 나이퀴스트 기준 아래에서 이미지를 획득해야 합니다. 이전에 보고된 바와 같이, 2.3배 이상 오버샘플링할 때 해상도에서 가장 큰 이점을 얻을 수 있습니다. 하지만 1.5배로 오버샘플링해도 SRRF-Stream+를 사용하면 여전히 좋은 결과를 얻을 수 있습니다.
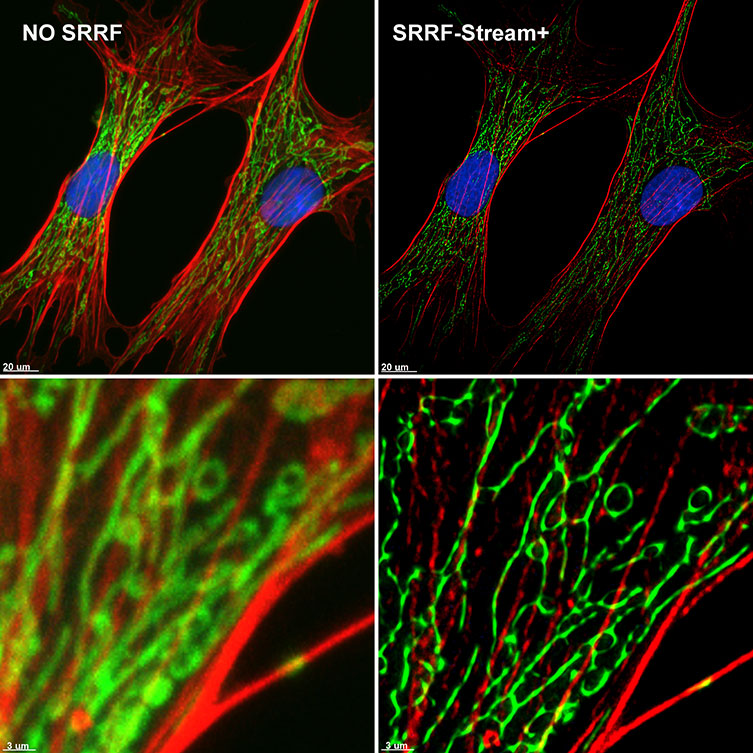
Figure 6 – SRRF-Stream+ delivers High-quality Super-resolved images. BPA cells stained with phalloidin (red), mitotracker (green) and DAPI (blue) where imaged with Ixon 888 Ultra in confocal mode (no SRRF) and confocal mode with SRRF-stream+
그림 1, 4, 5, 7을 분석해 보면 SRRF-Stream+의 이점은 분명하지만, 많은 잠재적 사용자들이 한 가지 의문을 품게 될 것입니다: 수집 속도는 어떤 영향을 받을까요? SRRF-Stream+가 6개 방향이 아닌 24개 방향의 반경을 계산하는 경우, SRRF-Stream+가 기존 버전의 SRRF보다 4배 느린가요? 새로운 SRRF 알고리즘을 개발할 때, 안도르는 많은 연구자들이 획득 속도 또한 필수적인 매개변수라는 점을 고려했습니다. 촬영 속도에 미치는 영향을 최소화하면서 이미지 품질을 개선하는 것이 가능했습니다. 이를 위해 CUDA 성능을 최적화하여 nVidia 그래픽 카드의 방대한 컴퓨팅 성능을 완벽하게 활용함으로써 SRRF-Stream+ 계산 속도를 높였습니다. 그 결과, 100개의 타임랩스와 각 타임포인트당 50개의 SRRF-Stream+ 이미지(총 500개의 이미지에 해당)를 캡처하는 경우, 기존 SRRF-Stream[2]과 비교할 때 캡처 시간은 0.5초 정도밖에 차이가 나지 않습니다.
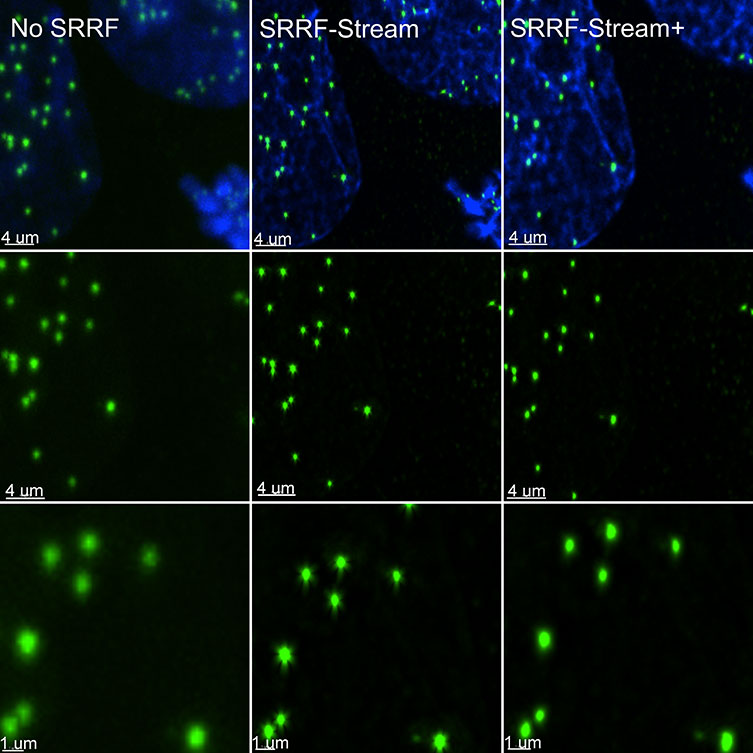
Figure 7 – SRRF stream+ delivers high-quality data. At very high magnifications, in specific structures, such has kinetochores some Star artefact could occasionally appear. SRRF-Stream+ radiality computation in 24 directions eliminates the star artefacts. Hela cells stained for Cenp-A (green-Kinetochore) and DAPI (blue-DNA) were imaged in the Dragonfly with an Ixon888 Ultra camera.
Andor의 기존 SRRF-Stream의 장점은 SRRF-Stream+에서도 그대로 유지되지만 이미지 품질이 개선되었습니다. 초고해상도 이미징 처리는 여전히 ImageJ SRRF('NanoJ-SRRF')보다 초고속 처리 속도(최대 30배 빠름)로 수행되며, 데이터 획득과 동시에 SRRF 이미지 획득/처리가 즉시 캡처됩니다. SRRF-Stream+ 알고리즘은 최종 해상도가 50~150nm인 이미지를 제공하며, 낮은 에너지 요구 사항으로 인해 라이브 세포 현미경 검사에 이상적인 솔루션입니다. 넓은 시야각으로 초고해상도 이미지를 획득할 수 있으며, 중요한 것은 초고해상도 현미경 검사가 세포 표면 이벤트에만 국한되지 않는다는 점입니다. SRRF-Stream+를 사용하면 세포나 조직 내부 깊은 곳의 초고해상도 이미지를 얻을 수 있으며 특별한 샘플 준비가 필요하지 않습니다.
SRRF-Stream은 출시 이후 많은 애플리케이션에 널리 사용되고 있습니다. 미세소관 불안정화를 통한 세포 말단으로의 미토콘드리아 이동 분석(5), 중간엽 줄기세포의 HIF1α 핵 전위 분석(6) 등이 iXon 카메라에서 SRRF-Stream을 사용한 예시입니다. 예를 들어, 광유전학적 도구를 사용한 세포 운동 분석(7)과 클라트린 의존성 소세포증 조절에서 클래스 II PI3K의 효과를 분석하는 소포 트래픽 연구(8)와 같은 SRRF-Stream 이미지 획득에도 Dragonfly 다중 모달 공초점 시스템이 사용되었습니다. SRRF-Stream+의 다른 응용 분야로는 세포 소기관 수준에서의 단백질 구조 분석, 세포 내부의 단일 분자 추적, 개별 SNARE 단백질 기계의 막 융합 연구, 세포 내 골격 재조립(액틴 섬유 그물망의 변화) 등이 있습니다.
결론적으로, 저희는 라이브 셀과 호환되는 초고해상도를 제공하는 SRRF-Stream 알고리즘을 개선하여 이전보다 훨씬 더 나은 결과를 제공합니다. SRRF-Stream+는 아티팩트 없이 세포 내 구조의 초고해상도 이미지를 제공하고, 카메라 고정 패턴 노이즈의 영향을 보정할 수 있으며, 고품질의 초고해상도 이미지를 제공합니다.
Bibliography
- Gustafsson, N., Culley, S., Ashdown, G. et al. Fast live-cell conventional fluorophore nanoscopy with ImageJ through super-resolution radial fluctuations. Nat Commun 7, 12471 (2016). https://doi.org/10.1038/ncomms12471
- Culley S, Tosheva KL, Matos Pereira P, Henriques R. SRRF: Universal live-cell super-resolution microscopy. Int J Biochem Cell Biol. 101:74-79 (2018). https://doi:10.1016/j.biocel.2018.05.014
- Browne M. Twelve Reasons Why Your Next Confocal Should Be Dragonfly. (2017) https://www.oxinst.com/assets/uploads/downloads/Dragonfly-Twelve-Reasons-Why.pdf
- Coates C, ‘SRRF-Stream’: Real-Time Super-Resolution in a Camera. (2017) https://andor.oxinst.com/assets/uploads/documents/srrf-stream-technical-note.pdf
- Choi, G.E., Oh, J.Y., Lee, H.J. et al. Glucocorticoid-mediated ER-mitochondria contacts reduce AMPA receptor and mitochondria trafficking into cell terminus via microtubule destabilisation. Cell Death Dis 9, 1137 (2018). https://doi.org/10.1038/s41419-018-1172-y
- Lee, H.J., Jung, Y.H., Oh, J.Y. et al. BICD1 mediates HIF1α nuclear translocation in mesenchymal stem cells during hypoxia adaptation. Cell Death Differ 26, 1716–1734 (2019). https://doi.org/10.1038/s41418-018-0241-1
- Castillo-Badillo J.A., Bandi A. C., Harlalka, and Gautam N. SRRF-Stream Imaging of Optogenetically Controlled Furrow Formation Shows Localised and Coordinated Endocytosis and Exocytosis Mediating Membrane Remodeling. ACS Synth. Biol. 9, 4, 902–919 (2020). https://doi.org/10.1021/acssynbio.9b00521
- Aung, K.T., Yoshioka, K., Aki, S. et al. The class II phosphoinositide 3-kinases PI3K-C2α and PI3K-C2β differentially regulate clathrin-dependent pinocytosis in human vascular endothelial cells. J Physiol Sci 69, 263–280 (2019). https://doi.org/10.1007/s12576-018-0644-2.
댓글
댓글 쓰기